
 129 usuarios conectados
129 usuarios conectados
/natureduca/quimica-las-disoluciones-la-composicion-de-las-disoluciones-01

Química
LAS DISOLUCIONES
La composición de las disoluciones - 1ª parte
La concentración de una disolución
 as propiedades de una disolución dependen de la
naturaleza de sus componentes y también de la proporción en la que éstos
participan en la formación de la disolución. La curva de calentamiento de una
disolución de sal común en agua, cambiará aunque sólo se modifique en el
experimento la cantidad de soluto añadido por litro de disolución.
as propiedades de una disolución dependen de la
naturaleza de sus componentes y también de la proporción en la que éstos
participan en la formación de la disolución. La curva de calentamiento de una
disolución de sal común en agua, cambiará aunque sólo se modifique en el
experimento la cantidad de soluto añadido por litro de disolución.
La velocidad de una reacción química que tenga lugar entre sustancias en disolución, depende de las cantidades relativas de sus componentes, es decir, de sus concentraciones. La concentración de una disolución es la cantidad de soluto disuelta en una cantidad unidad de disolvente o de disolución.
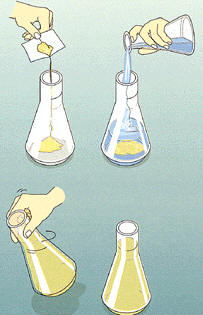
La preparación de una
disolución requiere calcular la cantidad de soluto necesaria para
conseguir la concentración deseada. Se añade el disolvente y se
agita o se calienta para obtener la disolución.
Formas de expresar la concentración
Existen diferentes formas dé expresar la concentración de una disolución. Las que se emplean con mayor frecuencia suponen el comparar la cantidad de soluto con la cantidad total de disolución, ya sea en términos de masas, ya sea en términos de masa a volumen o incluso de volumen a volumen, si todos los componentes son líquidos.
En este grupo se incluyen las siguientes:
Molaridad
Es la forma más frecuente de expresar la concentración de las disoluciones en química. Indica el número de moles de soluto disueltos por cada litro de disolución; se representa por la letra M. Una disolución 1 M contendrá un mol de soluto por litro, una 0,5 M contendrá medio mol de soluto por litro, etc.
El cálculo de la molaridad se efectúa determinando primero el número de moles y dividiendo por el volumen total en litros:
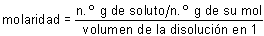
La preparación de disoluciones con una concentración definida de antemano puede hacerse con la ayuda de recipientes que posean una capacidad conocida. Así, empleando un matraz aforado de 0,250 litros, la preparación de una disolución 1 M supondrá pesar 0,25 moles de soluto, echar en el matraz la muestra pesada, añadir parte del disolvente y agitar para conseguir disolver completamente el soluto; a continuación se añadirá el disolvente necesario hasta enrasar el nivel de la disolución con la señal del matraz.
Gramos por litro
Indica la masa en gramos disuelta en cada litro de disolución. Tiene la ventaja de ser una concentración expresada en unidades directamente medibles para el tipo de disoluciones más frecuentes en química (las de sólidos en líquidos).
La balanza expresa la medida de la masa de soluto en gramos y los recipientes de uso habitual en química indican el volumen de líquido contenido en litros o en sus submúltiplos. Su cálculo es, pues, inmediato:
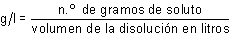

 © ASOCAE ONGD, Asociación Española para la Cultura, el Arte y la Educación -
www.asocae.org - RNA 592727 - CIF.: G70195805 ¦
Quiénes somos ¦
Contacto ¦
Bibliografía ¦
Política de privacidad ¦
Esta web NO utiliza cookies, ni guarda datos personales de los usuarios
© ASOCAE ONGD, Asociación Española para la Cultura, el Arte y la Educación -
www.asocae.org - RNA 592727 - CIF.: G70195805 ¦
Quiénes somos ¦
Contacto ¦
Bibliografía ¦
Política de privacidad ¦
Esta web NO utiliza cookies, ni guarda datos personales de los usuarios




